 뉴스센터
뉴스센터
![[코로나19 과학 리포트 2]_Vol.2 코로나19 변이체 vs 면역체계 방어시스템](https://www.ibs.re.kr:443/dext5data/2021/01/20210125_110606742_76737.jpg)
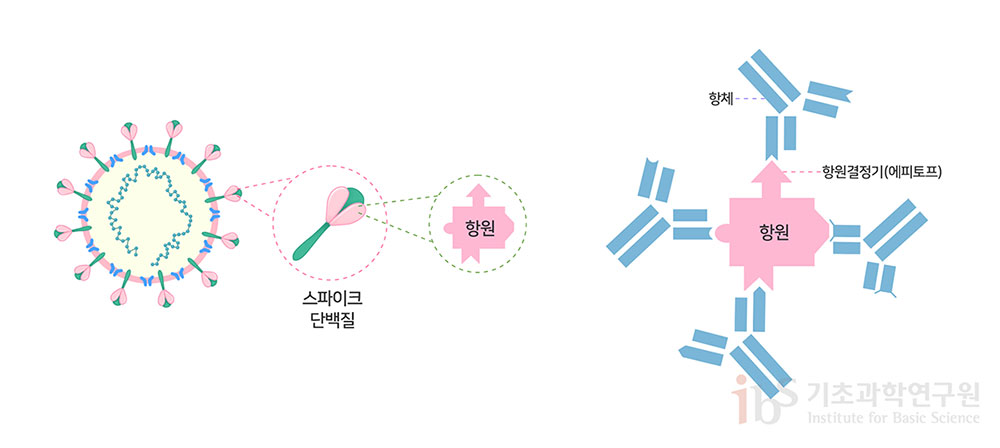
바이러스는 돌연변이를 통해 끊임없이 변화한다. 따라서 그 자체를 우려할 필요는 없다. 진화와 적응과정으로 인한 코로나19 바이러스의 다양화는 전 세계적으로 관찰된다. 새로 출현하는 대부분의 돌연변이는 바이러스에 선택적인 이점을 제공하지 않는다. 그러나 일부 돌연변이나 돌연변이 조합은 바이러스 생존에 유리한 성질을 발현시킨다. 예컨대, 수용체와의 결합력 증가로 세포 침투능력이 높아지거나, 항체가 인식하는 표면 구조를 변경해 숙주 면역반응의 회피 기능을 갖추는 것이 대표적이다. 일반적으로 많은 전염성 병원체는 숙주와 상호 공존하며 시간 경과에 따라 감염성은 증가하고 병원성은 감소한다. 바이러스 돌연변이가 나타날 때 다음과 같은 잠재적 결과를 고려할 수 있다. 첫째로 돌연변이로 인해 자연 또는 백신으로 인한 면역을 회피할 수 있거나, 사람에게 더 가볍거나 더 심각한 질병을 유발할 수 있다. 둘째로 돌연변이 때문에 바이러스가 사람들에게 더 빨리 퍼질 수 있고, 특정 진단 테스트에 의한 탐지를 어렵게 할 수 있다. 그러나 중합효소연쇄 반응(PCR)으로 바이러스를 검출할 때 여러 개의 표적(바이러스 유전자 부위)을 활용하므로, 돌연변이가 일부 표적을 변화시켜도 다른 표적은 여전히 작동한다. 사스코로나바이러스-2 돌연변이가 미칠 수 있는 영향을 상세히 알아보자. 바이러스 변이체, 면역체계 피할 수 있을까바이러스가 우리 몸의 면역을 회피할 만큼 충분히 변했다는 증거는 현재 없다. 그러나 B117은 팬데믹 기간 출현한 다른 버전의 바이러스와 다른 점이 있다. 아미노산 변화를 초래하는 17개의 돌연변이가 한꺼번에 생겼다는 것이다. 따라서 면역회피 가능성을 확인할 필요가 있다. 현재 접종 중인 백신은 면역계가 스파이크 단백질을 인식하고 차단할 수 있는 항체를 만들도록 설계되었다. 그러므로 스파이크 단백질이 변형되면 백신의 작동 방식이 달라질 수 있다. 스파이크 단백질은 1,273개의 아미노산 서열로 이루어진 거대 단백질이다. 항체는 항원의 3차 구조 일부분을 특이적으로 인식해서 만들어진다. 항체가 결합하는 항원의 특정 단편을 항원결정기 (epitope)라고 한다. 항원결정기는 대략 15개 아미노산 길이의 펩타이드 3차 구조라고 가정하면, 단일 스파이크 항원에 대해서 유도될 수 있는 항체는 수백 종류가 넘는다. 백신을 접종하면 다양한 방식으로 결합하는 다양한 항체를 생성한다(그림 1). 단일 항원에 대해 다양한 종류의 “다클론성 항체(polyclonal antibody)”가 생성되기 때문에 D614G, N501Y와 같은 점돌연변이가 몇 개 발생해도 백신의 효능에 크게 영향을 미칠 가능성은 적다.
다행히 최근 화이자의 백신이 영국과 남아공에서 퍼진 변이 바이러스에도 효과가 있다는 연구결과가 나왔다(그림 2).
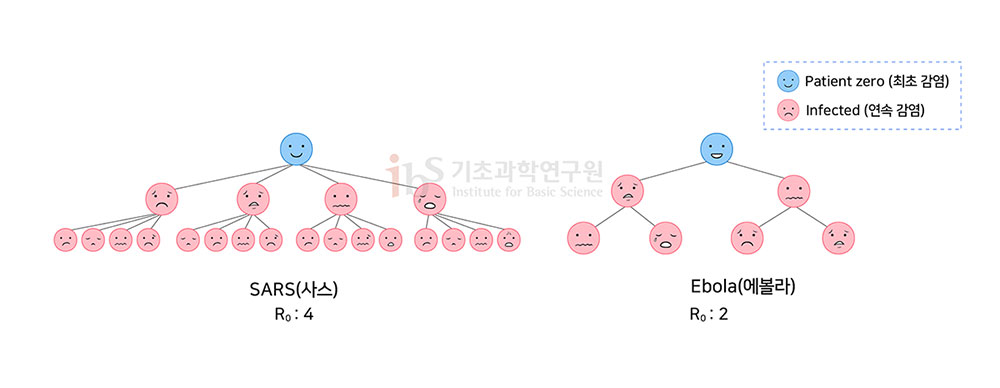
스파이크를 표적으로 삼는 항체 기능을 다소 잃더라도 백신은 바이러스를 차단하는 다른 방법을 가지고 있다. 백신은 항체와 더불어 후천면역의 양대 축인 T 세포를 활성화한다. 바이러스 돌연변이가 이 같은 여러 겹의 인체 면역 무기를 극복하기는 어려울 것이다. RNA기반 백신, 플랫폼 활용한 ‘업데이트’ 용이사스코로나바이러스-2가 단기간에 백신을 무력화할 만큼 진화할 것 같지는 않다. 그러나 장기적으로 돌연변이가 계속 누적되면 이를 방어하기 위한 백신의 업데이트가 필요하다. 점차 더 많은 사람들이 백신을 접종받으면서 바이러스에 대한 진화적 압력이 증가하여 돌연변이 발생이 빨라질 것이다. 백신에 적응하는 바이러스의 변이와 진화가 발생하는 것은 자연스러운 일이다. 현재 개발된 코로나19 백신은 스파이크를 암호화하는 RNA와 DNA 절편을 접종하는 형태이다. 생백신, 사백신, 혹은 단백질 백신보다 RNA/DNA를 기반으로 하는 백신(화이자, 모더나, 아스트라제네카, 얀센 백신 등)은 업데이트가 쉽다는 장점이 있다. 백신 개발 플랫폼은 기존 그대로 이용하면서 돌연변이에 대응하여 맞춤형으로 염기서열을 바꾸기만 하면 된다. 변이 바이러스는 감염자를 더 아프게 하는가D614G, B117 돌연변이를 포함하여 코로나19 발생 시점부터 지금까지 발생한 돌연변이가 질병 증상에 영향을 미친다는 증거는 없다(Volz et al., 2020, Rambaut et al., 2020). B117과 관련하여 감염 증상이 더 심각해졌다는 징후는 관찰되지 않았다. 그럼에도 영국의 대부분 감염 사례가 중증 증상의 발생 가능성이 낮은 60세 미만 사람들에게서 확인되었기 때문에 돌연변이와 감염 심각성의 연관성을 평가하기는 어렵다(ECDC 2020). B117 돌연변이체 감염 환자의 입원 비율과 체류 기간 및 사망률을 분석해야 한다. 현재까지 보고된 병원 입원과 사망률은 모두 후행 지표이며 정확한 평가를 위해서는 수개월 이상이 필요하다. 코로나19 감염 중증도는 주로 병독성 인자인 외피 단백질의 성격에 의해 결정된다. 외피 단백질이 결손 또는 변형되면 병독성이 약화된다. B117에서 Q27정지 돌연변이로 인해 C-말단 대부분이 손실된 비정상 단백질이 만들어진다. 또한 C 말단의 마지막 4개의 아미노산(73, 74, 75, 76 번째 위치) 서열은 병독성을 결정하는 중요한 인자이다. 그러므로 73번째 위치에서 일어난 Y73C 돌연변이도 병독성에 영향을 줄 것으로 예상된다. 결론적으로 Q27정지 및 Y73C 돌연변이는 병독성을 약화시켜, B117 감염자에서는 증상이 미약하게 나타날 것이다. “B117 환자에서 감염 증상이 더 심각해진 징후는 없다”라는 소극적 자세를 지양하고, 감염 증상의 약화 여부에 대해 신속하고 적극적인 검증을 할 필요가 있다. 더 빠르게 전파되는가전파력이 높아지면 감염자수와 사망자수가 늘어날 수 있다. D614G 및 B117 변이체가 코로나19 질병의 중증도, 백신 효능에 영향을 미친다는 직접적인 증거는 없다. 그러나 모델링 및 세포 수준의 연구 결과는 바이러스 전파 속도를 높일 수 있음을 암시한다. 2020년 7월 초 미국 연구진은 D614G로 알려진 돌연변이가 코로나19 바이러스의 전파력을 6배 증가시킨다는 연구 결과를 발표했다(Korber et al., 2020). 이는 가상 바이러스와 배양 세포 수준의 실험실 조건에서 얻은 결과를 바탕으로 과장하여 추론한 것이었음이 밝혀졌다. 후속 연구에 의하면 전파력이 약간 증가하였을 뿐이다(2020 Cell). 최근 영국 연구자들은 B117이 다른 버전의 코로나바이러스보다 50%에서 70% 더 전염성이 있다고 추정하고 있다. 전문가들은 B117이 R-naught (R0) 값을 1.1에서 1.5로 증가시켰을 수 있다고 예상한다(GOV.UK 2020). R0 값이 1보다 크면 전염병이 증가하고 1보다 작으면 축소된다. 그러므로 0.4 증가했다는 것은 우려할만하다. 전자는 평균 10명의 감염된 사람이 11명의 새로운 감염으로 이어지지만, 후자는 15명의 새로운 감염이 발생한다. 2차, 3차 새로운 감염이 발생함에 따라 그 차이는 기하급수적으로 커진다(그림 3).
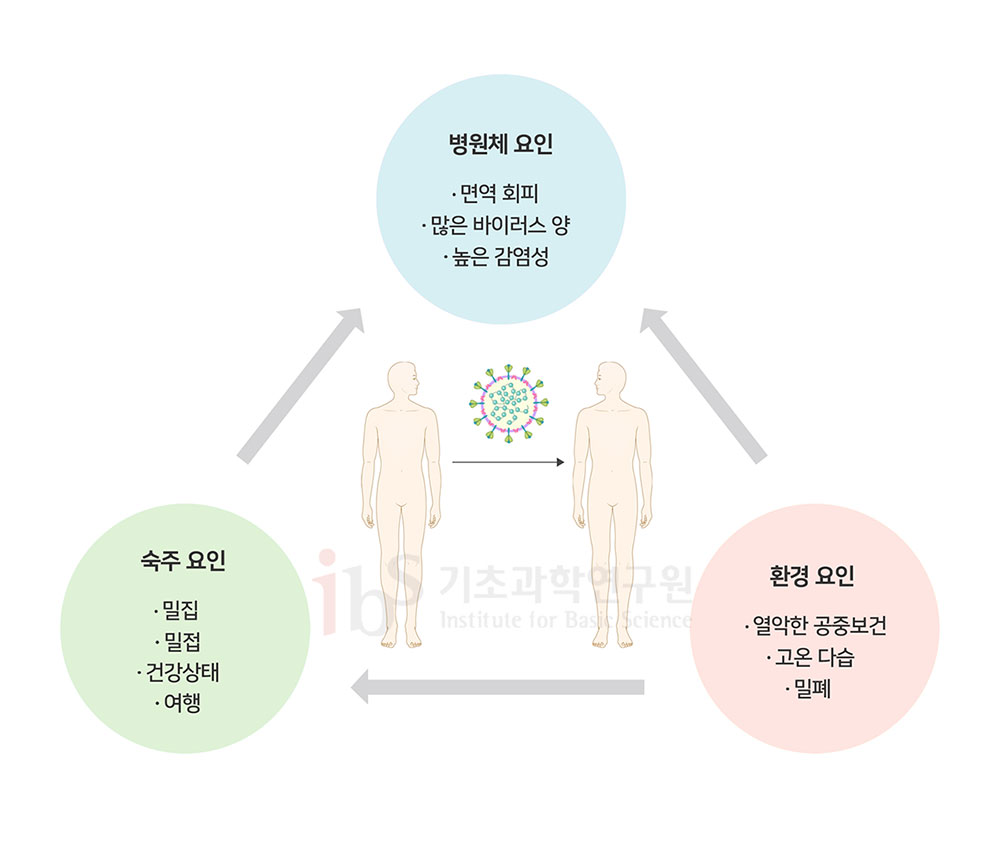
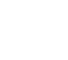
N501Y 돌연변이는 바이러스가 ACE2 수용체에 더 잘 붙도록 돕는 것으로 나타났다(Starr et al., 2020). 또 다른 돌연변이 P681H는 바이러스의 퓨린 절단 부위에 영향을 미쳐 바이러스의 세포 침입능력을 높여준다(Hoffmann et al., 2020; Peacock et al., 2020). 영국 정부 자문위원이자 바이러스 학자인 웬디 바클레이 박사는 전파력 증가가 부분적으로는 B117이 다른 버전의 바이러스에 비해 더 높은 비율로 어린이를 감염시킨 결과일 수 있다고 말한다. 어린이는 성인보다 사스코로나바이러스-2 감염에 더 강한 저항성을 나타낸다. 아이들이 성인보다 기도 세포에 ACE2 수용체가 많지 않기 때문으로 추정된다. B117이 다른 변이체보다 ACE2에 더 잘 붙는다면 감염을 위해 많은 수용체가 필요하지 않을 것이다. 최근 영국에서 주로 발표된 B117 돌연변이체 관련 통계, 역학 자료 분석 결과가 B117이 다른 버전의 코로나바이러스보다 전파력이 높다는 확실한 증거는 아니다. 물론 전파력 70% 증가 및 R0값 0.4 증가 수치는 B117 변이체의 고유 성질로부터 기인한 것일 수 있다. 하지만 영국의 특수한 코로나19 대응 방식과 사회적 요인을 반영한 결과일 수도 있다. R0 값은 특정 감염병 고유의 값이 아니다. 단위 시간당 접촉 숫자는 시골보다 대도시에서 훨씬 많으므로 인구 밀집 지역에서 조사를 하면 R0값이 더 높게 나온다. 전염병 유행의 전파 속도는 R0, 연속감염기간(증상발현 후 다음 감염자 증상발현까지의 시간), 인구 밀도, 역학조사 방식, 사회적 요인 등에 의해 복합적인 영향을 받는다. 또한 수학적 모델에 근거한 돌연변이와 전파력 향상과의 상관관계가 실제 사람 간 감염과 전파에 그대로 적용 가능한지도 단언할 수 없다. 동물모델을 이용한 역학 실험, 바이러스학, 유전체학, 모델링 등 다양한 증거들을 수집해야 돌연변이와 전파 속도의 상관관계가 명확해질 것이다. 백신 접종 늘수록 변이 현상 잘 감시해야팬데믹 진행 과정에서 ‘바이러스 돌연변이’를 주목해야 할 때와 그렇지 않아도 될 때가 있다. 돌연변이는 바이러스가 종간장벽을 돌파해서 인수공통감염을 일으키는 데 필요한 사건이다. 돌연변이 때문에 코로나19가 박쥐에서 인간으로 옮겨왔다. 그러므로 중간 숙주에 머무는 바이러스의 돌연변이는 주목해야 한다. 팬데믹 동안 발생하는 돌연변이는 바이러스가 숙주에 적응해나가는 과정이다. 대부분의 돌연변이는 바이러스 자신에게도 해롭다. 바이러스에 이롭게 작용하는 돌연변이도 한 번의 돌연변이에 의해서 확립되지 않는다. 몇 세대 동안 연속해서 성공적으로 일어나야 한다. 역사적으로도 팬데믹 진행 중에 돌연변이가 질병에 치명적 영향을 준 사례는 드물다. 인플루엔자는 코로나바이러스보다 더 빠르게 돌연변이가 일어나며, 훨씬 많은 변이체가 존재했다. 하지만 지난 1세기 동안 인플루엔자 병원성은 더 악화되지 않았다. 자연 감염 혹은 백신 접종으로 면역이 생기면 면역회피를 위해 바이러스 돌연변이가 촉진된다. 백신 출시에 따라 경계를 유지하고 새로운 돌연변이를 계속 감시해야 한다. 인플루엔자와 HIV는 백신을 피하면서 계속 돌연변이를 일으키고 있다. 사스코로나바이러스-2의 치명적 변이는 아직 발생하지 않은 것으로 보인다. 만약 바이러스의 스파이크 단백질이 크게 변한다면 백신 기능을 떨어뜨릴 수 있다. 바이러스의 완전 박멸은 어렵더라도 전파 속도만큼은 늦춰야 한다. 그러면 돌연변이 시계도 늦출 수 있다. 확산을 줄이면 변이 확률이 낮아진다. 사스코로나바이러스-2, 기존 진화 규칙 따를 듯팬데믹과 바이러스의 역사를 살펴보면, 대개 바이러스는 돌연변이로 인해 전파력은 증가되고 병독성은 약화된다. 영국발 B117 변이체도 이러한 규칙을 따를 것으로 예상된다. 스파이크 단백질의 돌연변이는 ACE2 수용체와의 친화력을 증가시켜 세포 감염을 쉽게 하는 반면, 외막 단백질의 Q27정지 돌연변이는 바이러스의 독성을 약화시킬 수 있다. 예측대로 영국발 B117 변이체가 전파력은 증가하고 독성은 약해진 것이라면, 오히려 바이러스 종식에 청신호다. 전파력 증가를 우려하는 이유는 감염자 증대가 의료체계 포화 및 중증 환자 관리 난항을 유발하기 때문이다. 전파력은 바이러스 특성과 돌연변이에 의해 일부 영향을 받지만, 동시에 인간행동과 주변 환경 조건에도 영향을 받는다. 후자는 사람이 통제할 수 있는 영역이다(그림 4). 자연스럽게 발생하는 돌연변이를 막을 방법은 없다. 인간이 할 수 있는 일은 돌연변이를 가속하는 상황을 조성하지 않는 것이다. 여전히 환기, 손씻기, 마스킹, 사회적 거리 두기는 B117 예방과 새로운 돌연변이 발생 시계를 늦추는 유효한 수단이다. R0값은 마스크 쓰기와 거리 두기와 같은 적극적 행동으로 낮출 수 있다.
2020년 7월 초 D614G 변이체가 6배 전파속도를 증가시킨다는 논문을 보고 각종 언론매체가 경쟁적으로 보도를 쏟아냈다. 우리는 그로 인해 큰 혼란을 겪었던 것을 기억한다. 더 나쁜 상황을 대비해서 돌연변이에 주목할 필요는 있다. 하지만 과학적 사실을 앞서가는 주관적 과장은 불필요한 불안과 공포를 조성할 뿐이다. 우리는 과도한 공포와 안이한 대응 모두를 경계해야 한다. 과학적 사실에 근거한 냉철한 균형감각을 갖추도록 노력해야 할 것이다. ▣ 참고문헌Choi et al., Persistence and Evolution of SARS-CoV-2 in an Immunocompromised Host. N Engl J Med 2020; 383:2291-2293 COVID-19 Genomics UK Consortium (COG-UK) 2020. Available from: https://www.cogconsortium.uk/. European Centre for Disease Prevention and Control (ECDC). COVID-19 surveillance report. Week 50, 2020. Stockholm: ECDC. Available from: https://covid19-surveillancereport.ecdc.europa.eu/. GOV.UK. Speech: Prime Minister's statement on coronavirus (COVID-19): 2020 Available from: https://www.gov.uk/government/speeches/prime-ministers-statement-on-coronaviruscovid-19-19-december-2020. GISAID. 2020. Available from: https://www.gisaid.org/. Hoffmann, Markus, Hannah Kleine-Weber, and Stefan Pöhlmann. 2020. “A Multibasic Cleavage Site in the Spike Protein of SARS-CoV-2 Is Essential for Infection of Human Lung Cells.” Molecular Cell 78: 779–84.e5. Korber et al., Spike mutation pipeline reveals the emergence of a more transmissible form of SARS-CoV-2. Cell 2020 182:812-827. Laussauniere et al., Working paper on SARS-CoV-2 spike mutations arising in Danish mink, their spread to humans and neutralization data. SARS-CoV-2 spike mutations arising in Danish mink and their spread to humans. Copenhagen: Statens Serum Institut; 2020. Available from: https://files.ssi.dk/Mink-cluster-5-shortreport_AFO2. Oude Munnink et al., Transmission of SARS-CoV-2 on mink farms between humans and mink and back to humans. Science. 2020:eabe5901. Peacock, Thomas P., Daniel H. Goldhill, Jie Zhou, Laury Baillon, Rebecca Frise, Olivia C. Swann, Ruthiran Kugathasan, et al. 2020. “The Furin Cleavage Site of SARS-CoV-2 Spike Protein Is a Key Determinant for Transmission due to Enhanced Replication in Airway Cells.” Cold Spring Harbor Laboratory. https://doi.org/10.1101/2020.09.30.318311 Rambaut et al., Preliminary genomic characterisation of an emergent SARS-CoV-2 lineage in the UK defined by a novel set of spike mutations: COVID-19 genomics UK consortium; 2020. Available from: https://virological.org/t/preliminary-genomic-characterisation-of-an-emergent-sars-cov-2-lineage-in-the-ukdefined-by-a-novel-set-of-spike-mutations/563. Starr, Tyler N., Allison J. Greaney, Sarah K. Hilton, Daniel Ellis, Katharine H. D. Crawford, Adam S. Dingens, Mary Jane Navarro, et al. 2020. “Deep Mutational Scanning of SARS-CoV-2 Receptor Binding Domain Reveals Constraints on Folding and ACE2 Binding.” Cell 182: 1295–1310.e20. Tegally et al., Emergence and rapid spread of a new SARS-CoV-2 lineage with multiple spike mutations in South Africa. medRxiv 2020 doi: https://doi.org/10.1101/2020.12.21.20248640. Volz et al. Evaluating the Effects of SARS-CoV-2 Spike Mutation D614G on Transmissibility and Pathogenicity. Cell. 2020. doi:10.1016/j.cell.2020.11.020. 글 | 안광석 기초과학연구원(IBS) RNA 연구단 연구위원‧서울대 생명과학부 교수(바이러스면역학) 편집 | IBS 커뮤니케이션팀 발행일 | 2021년 1월 15일 본 글의 저작권은 기초과학연구원에 있습니다. 무단 전재를 금지하며 공유, 인용 및 재사용 시에는 출처를 명시해주시기 바랍니다. |
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- :
- 최종수정일 2023-11-28 14:20